La ley de los gases ideales es la ecuación de estado del gas ideal, un gas hipotético formado por partículas puntuales, sin atracción ni repulsión entre ellas y cuyos choques son perfectamente elásticos (conservación de momento y energía cinética). Los gases reales que más se aproximan al comportamiento del gas ideal son los gases monoatómicos en condiciones de baja presión y alta temperatura.

Empíricamente, se observan una serie de relaciones entre la temperatura, la presión y el volumen que dan lugar a la ley de los gases ideales, deducida por primera vez por Émile Clapeyron en 1834.
La ecuación que describe normalmente la relación entre la presión, el volumen, la temperatura y la cantidad (en moles) de un gas ideal es:
Donde:
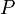 = Presión
= Presión = Volumen
= Volumen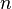 = Moles de Gas.
= Moles de Gas.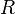 = Constante universal de los gases ideales .
= Constante universal de los gases ideales .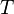 = Temperatura absoluta
= Temperatura absoluta
Ley de Boyle:
“El volumen de un gas, a temperatura constante, es inversamente proporcional a la presión”
Ley de Charles:
“El volumen de un gas a presión constante es directamente proporcional a la temperatura kelvin”.
Ley de Gay-Lussac
Cuando se investiga experimentalmente como depende entre sí el volumen y la temperatura de un gas a una presión fija, se encuentra que el volumen aumenta linealmente al aumentar la temperatura. Esta relación se conoce como Ley de Charles y Gay-Lussac, y se puede expresar algebraicamente por:
V = V0(1 + "t)

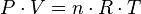
Gracias :)
ResponderEliminarMuy interesante como resuelve ejercicios, pero conozco un sitio wed, donde resuelven también otros ejercicios se lo recomiendo se llama profecasa.com
ResponderEliminarDeja de mamar.
Eliminarbuena informacion pero as algo mas interesanta
ResponderEliminar